具体内容
若移植物中同种异型反应性T细胞识别宿主同种异型组织抗原而诱发针对受者的排斥反应,此为移植物抗宿主反应(GVHR)。
GVHR主要见于骨髓移植后,是影响骨髓移植成功的首要因素,也可见于胸腺、小肠和肝移植以及免疫缺陷个体接受大量输血时。
发生条件
(1)宿主与移植物之间的组织相容性不合;
(2)移植物中必需含有足够数量的免疫细胞;
(3)宿主处于免疫无能或免疫功能严重缺损状态。
临床表现
受者对供者组织器官产生的排斥反应称为宿主抗移植物反应(HVGR)根据移植物与宿主的组织相容程度,以及受者的免疫状态,移植排斥反应主要表现为三种不同的类型。
超急排斥(hyperacute rejection)反应一般在移植后24小时发生。目前认为,此种排斥主要由于ABO血型抗体或抗Ⅰ类主要组织相容性抗原的抗体引起的。受者反复多次接受输血,妊娠或既往曾做过某种同种移植,其体内就有可能存在这类抗体。
在肾移植中,这种抗体可结合到移植肾的血管内皮细胞上,通过激活补体有直接破坏靶细胞,或通过补体活化过程中产生的多种补体裂解片段,导致血小板聚集,中性粒细胞浸润并使凝血系统激活,最终导致严重的局部缺血及移植物坏死。
超急排斥一旦发生,无有效方法治疗,终将导致移植失败。因此,通过移植前ABO及HLA配型可筛除不合适的器官供体,以预防超急排斥的发生。
急性排斥(acute uejection)是排斥反应中最常见的一种类型,一般于移植后,进行迅速。肾移植发生急性排斥时,可表现为体温度升高、局部胀痛、肾功能降低、少尿甚至无尿、尿中白细胞增多或出现淋巴细胞尿等临床症状。
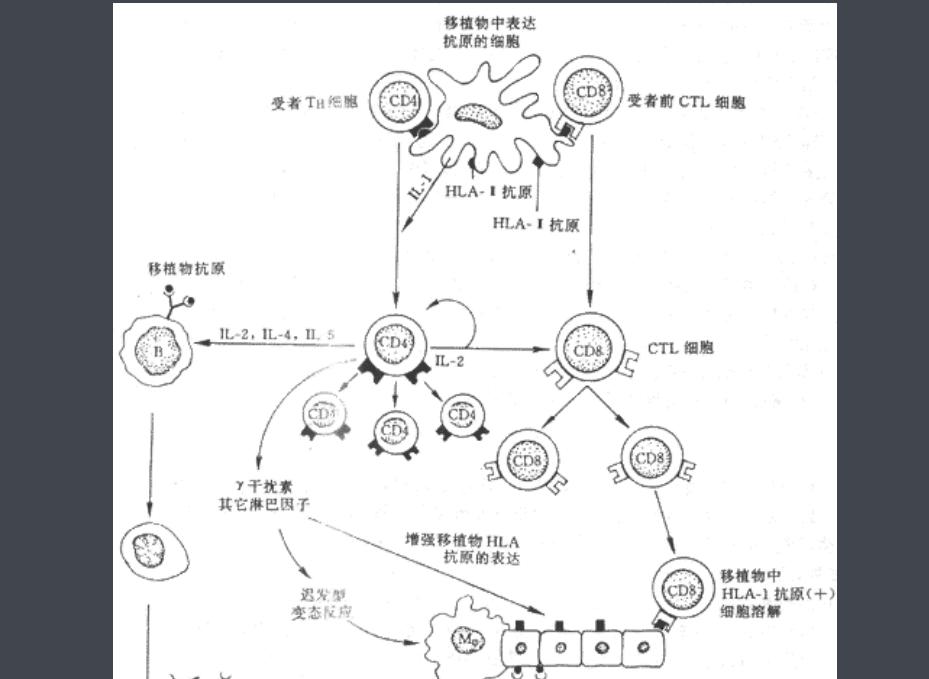
细胞免疫应答是急性移植排斥的主要原因,CD4+T(TH1)细胞和CD8+TC细胞是主要的效应细胞。即使进行移植前HLA配型及免疫抑制药物的应用,仍有30%~50%的移植受者会发生急性排斥。大多数急性排斥可通过增加免疫抑制剂的用量而得到缓解。
慢性排斥(chronic rejection)一般在器官移植后数月至数年发生,主要病理特征是移植器官的毛细血管床内皮细胞增生,使动脉腔狭窄,并逐渐纤维化。
慢性免疫性炎症是导致上述组织病理变化的主要原因。目前对慢性排斥尚无理想的治疗措施。
治疗
环孢素可用于治疗急性或慢性GVHD,可单独或在原有糖皮质激素的基础上加此药,其用法为每日2-3mg/kg分2次口服,待病情稳定后缓慢减药。对肝移植手术时,为预防发生GVHD,应给予他克莫司(tacrolimus),其用法为每日0.1-0.2mg/kg,分2次口服,在术后6小时开始应用。对肾移植的患者用他克莫司的用法,为每日0.15-0.3mg/kg,分2次口服。
局部外用他克莫司、吡美莫司治疗皮疹有效。其他如甲氨蝶呤,麦考酚酸酯,糖皮质激素,硫唑嘌呤,沙利度胺等免疫抑制剂或免疫调节剂也可用来阻止发病。可使GVHD的发生率降低。有报道称,PUVA单用或与甲氨蝶呤合用,治疗慢性GVHD有效。阿维A对慢性GVHD的硬皮病样皮损有效。
急性GVHD可用抗胸腺细胞球蛋白,其用量一般成人每日15-30mg/kg,通过大静脉滴注。治疗GVHD的重点是预防,尽量减少发生GVHD的危险因素。对免疫缺陷或免疫抑制者输血或血制品时,要先经放射线照射后再应用。
针对细胞因子的单克隆抗体、丙种球蛋白注射、体外光分离置换法(extra‐corporeal photopheresis)、免疫毒素、受体拮抗剂等,有些已经用于临床,或将来可能用于临床。
预后
急性一旦发生,存活率与病变程度有关。轻度可自行消退。中-重度经治疗可得到改善,45%是骨髓移植的主要死因。进行性间质性肺炎是其中常见的死因。
慢性GVHD6年存活率20~70%,10年总生存率为42%。
轻度的GVHD具有移植物抗白血病的作用,可明显减少白血病的复发。