定律定義
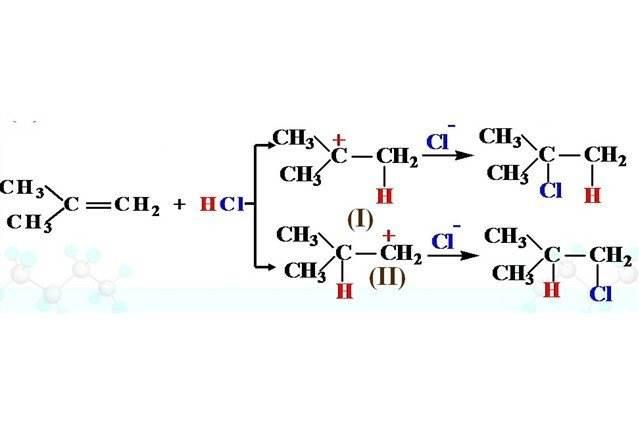
馬爾科夫尼科夫規則(Markovnikov's rule)簡稱“馬氏規則”。它是指有機反應中的一條規律。1870年由馬爾科夫尼科夫發現。馬氏規則規定:在烯烴的親電加成反應中,加成試劑的正性基團将加到烯烴雙鍵(或三鍵)帶取代基較少(或含氫較多)的碳原子上 。它闡明了在加成試劑與烯烴發生反應中,如可能産生兩種異構體時,為何往往隻産生其中的一種。例如,在鹵化氫對異丁烯的加成反應中,HX 的正離子H連接到雙鍵末端的碳原子上,形成叔鹵代物:
馬氏規則的這種具有選擇性的加成稱為區位選擇,可以用電子效應來闡明 。帶正電荷部分的Y首先進攻雙鍵,它傾向于加成到雙鍵中電子密度較高的一端,同時所生成的碳正離子一端帶有取代基:
由于烷基的超共轭穩定作用,有利于正電荷的分散,結構式a比b穩定,是加成反應的主要方向。因此,馬氏規則可以用來預示親電加成反應的方向。馬氏規則可用另一種方法表述:不對稱烯烴與極性試劑加成時,試劑中正離子或帶部分正電荷部分加到重鍵中帶有部分負電荷的碳原子上,而試劑中負離子或帶部分負電荷部分加到重鍵中帶有部分正電荷的碳原子上。如此表述,不僅适用于不含氫原子的加成試劑,也适用于分子中含有吸電基的不飽和烴的衍生物。
在自由基加成反應中,加成試劑對烯烴的加成位置往往與馬氏規則不一緻。例如,在溴化氫對異丁烯的加成反應中,若在過氧化物的作用下,則溴原子連接到末端碳原子上,而不是按馬氏規則所預示那樣,連在第二碳原子上,結果得到2-甲基溴丙烷:
這一現象稱為過氧化物效應。造成這種現象的原因是:在上述自由基加成反應中,首先進攻雙鍵的試劑是Br·。由于生成自由基的穩定性不同,二級碳自由基因受兩個甲基的超共轭穩定作用,要比一級碳自由基的穩定性大,故前者成為加成反應的主要方向。
産生原因
馬氏規則的原因是親電加成反應中生成了較為穩定的碳正離子。加上一個H+的碳原子會使其他碳原子上引入一個正電荷,形成一個碳正離子。由于誘導效應和超共轭效應,取代基(碳上連接的碳或給電子基團)越多的碳正離子越穩定。而加成反應的主要産物會由一個更加穩定的中間體産生。所以烯烴加溴化氫時,溴化氫中的氫總是加在連氫最多的碳上,而鹵素基團加在連氫最少的碳上。然而,其它比較不穩定的碳正離子仍然存在,通過它們生成的産物是不符合馬氏規則的,通常是反應的副産物。
這個規則可以概括為“氫多加氫”或“富者愈富,而窮者愈窮”:連氫多的碳會得到另外的氫,而連氫少的碳會得到另外的取代基。對于其他不對稱親電試劑也是如此。正電基團加到取代少的碳上,負電基團加到取代多的碳上。
發展簡史
馬爾科夫尼科夫(Markovnikov)用于證明其規則的一個反應是碘化氫和溴乙烯的加成。根據他的規則,鹵素将會加在已經有一個鹵素的碳上。而這個産物(1-碘-1-溴乙烷)是偕鹵化物水解反應的産物。用潮濕的氧化銀處理這個産物則會得到乙醛,證明了産物的結構。有人認為,在1869年馬爾科夫尼科夫的論文是粗心的,因為他自己沒有做很多實驗。這個規則僅僅作為了一個四頁長的腳注出現于一篇26頁的文章中。因此他的規則經過了大約60年才被廣泛認可。
最初,馬氏規則應用于普通烯烴與鹵化氫的親電加成反應,氫原子加在了含氫較多的碳原子上。但是,當烯烴雙鍵上連接了具有吸電子誘導效應的基團時,氫原子加在了含氫較少的碳原子上。雖然加成取向不同,但它們本質上都符合馬氏規則。後來,由于反應物結構和反應試劑的多樣性且反應機理各異,最終總結出了廣義的馬氏規則。